بارم بندی شیمی دبیرستان و پیش دانشگاهی
 برای دریافت بارم بندی شیمی مقاطع متوسطه و پیش دانشگاهی بر روی لینک زیر کلیک کنید
برای دریافت بارم بندی شیمی مقاطع متوسطه و پیش دانشگاهی بر روی لینک زیر کلیک کنید
 برای دریافت بارم بندی شیمی مقاطع متوسطه و پیش دانشگاهی بر روی لینک زیر کلیک کنید
برای دریافت بارم بندی شیمی مقاطع متوسطه و پیش دانشگاهی بر روی لینک زیر کلیک کنید
رادیواکتیویته اولین بار در سال 1896 توسط دانشمند فرانسوی، هنری بکرل (Henri Becquerel) در زمانی که بر روی مواد فسفرسنت ( فسفرسنت چیزی است شبیه فلوئورسنت ) تحقیق میکرد، کشف شد. اگر این مواد در معرض نور قرار بگیرند، در تاریکی تابش میکنند. بکرل گمان میکرد که تابش اشعه X تولید شده در لوله های کاغذ به نحوی به فسفرسنت ارتباط دارد. برای یافتن این ارتباط او آزمایشی ترتیب داد.
صفحهی عکاسی را در کاغذ سیاه گذاشت و کنار مواد فسفرسنت مختلف قرار دارد. همه جوابها منفی بود. هیچ یک از مواد مورد آزمایش اثری بر صفحه عکاسی نگذاشتند، این بار بکرل نمک های اورانیوم را آزمایش کرد. نتایج نشان میداد که این ترکیبات اثر شدیدی روی صفحهی عکاسی میگذارند.
در هر صورت به زودی مشخص شد که سیاه شدن صفحهی عکاسی، هیچ ارتباطی با مواد فسفرسنت ندارد، چون این مواد، در تاریکی صفحه عکاسی را تیره کرده بودند. علاوه بر آن نمک های غیر فسفرسنت اورانیوم و حتی اورانیوم فلزی نیز صفحهی عکاسی را تیره کرده بود. مشخص است که نوع جدیدی از تابش که قابلیت عبور از کاغذ سیاه را هم دارد، باعث تیره شدن صفحه عکاسی شده بود. البته بسیاری بر این عقیده اند که هانری بکرل به طور کاملاً تصادفی موفق به کشف رادیواکتیو شده است.
در ابتدا تصور میشد که این تابش جدید نیز مشابه پرتو x است. اما تحقیقات بیشتر توسط پیشگامان علوم هسته ای یعنی بکرل، پیرکوری (Piere Curie) ماری کوری ( Marie Curie ) ، ارنست رادرفورد (Ernest Rutherford) نشان داد که رادیواکتیویته بسیار پیچیده تر از چیزی است که تصور میشد. پس از آن با ادامهی تحقیقات دانشمندان در سال 1911 رادفورد وجود هسته را در اتمها اعلام کرد.
محققان هم چنین دریافتند که عناصر شیمیایی دیگر نیز ایزوتوپ های رادیواکتیو دارند. رادیواکتیویته به ماری کوری کمک کرد تا رادیوم و باریوم را که از نظر خواص شیمیایی بسیار به هم شبیهند و تشخیص آنها دشوار است، از هم جدا کند. اما مدتها طول کشید تا دانشمندان به خطرات تشعشعات رادیواکتیو پی ببرند.

آنها حتی نمی دانستند که اگر این مواد وارد بدن انسان شود همچنان به تشعشع خود ادامه میدهد و در اکثر موارد باعث ابتلاء فرد به سرطان و دیگر مشکلات وخیم خواهد شد. حتی بسیاری از پزشکان مواد رادیواکتیو را به عنوان دارو به بیماران خود تجویز میکردند.
ماری کوری پیش از مرگش علیه این نوع درمان سخنرانی کرد و درباره اثرات ناشناختهی تشعشعات روی بدن انسان هشدار داد.جالب آن که علت مرگ ناگهانی وی نیز به این علت بود که در معرض تشعشعات مواد رادیواکتیو قرار داشت و این در حالی بود که تا آن زمان اثرات مضر اشعه ی رادیو اکتیو ناشناخته بود.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ترکيب |
نقطه ذوب |
|
NaCl |
8010C |
|
MgO |
25820C |
|
NaBr |
4740C |
|
LiF |
840C |




 آلومنيوم فسفات = AlPO4
آلومنيوم فسفات = AlPO4
آمونيوم سولفيد = (NH4)2S
باريم هيدروکسيد = Ba(OH)2
منيزيم فسفات = Mg3(PO4)2
سولفيت(IV)سرب = Pb(SO3)2
استرنسيم کربنات = SrCO3
روي فسفات = Zn3(PO4)2
آمونيوم اکسيد= (NH4)2O
کلسيم نيترات = Ca(NO3)2
سولفات(II)تنگستن= WSO4
 مرحله ۱ :
مرحله ۱ : در صورتيکه ضرايب اعمال شده، قابليت ساده کردن را داشته باشد آنها را تاکوچکترين عدد صحيح ساده مي کنيم. اکسيد آلومنيوم قابليت ساده کردن ندارد.
در صورتيکه ضرايب اعمال شده، قابليت ساده کردن را داشته باشد آنها را تاکوچکترين عدد صحيح ساده مي کنيم. اکسيد آلومنيوم قابليت ساده کردن ندارد. فسفيدسديم = Na3P
فسفيدسديم = Na3P
فسفيد (III) آهن= FeP
سولفيد(II)مس= CuF2
سولفيد(I) نقره = Ag2S
نيتريد (II) منگنز= Mn3N2
يديد(II) سرب= PbI2
برميد (II) مس= CuBr2
فسفيد (II) ظلاي= Au3P2
اکسيد (IV)سرب= PbO2
نيتريت (I) نقره = Ag3N
کلريد (II) مس= CuCl2
منيزيم فلوئوريد = MgF2
آلومينيوم سولفيد = Al2S3
کلسيم نيتريد = Ca3N2
باريم يديد = BaI2
پتاسيم برميد = KBr
آلومينيوم فسفيد = AlP
استرنسيوم اکسيد = SrO
منيزيم نيتريد = Mg3N2
سزيم فسفيد = Cs3P
 وقتي که دو يا چند اتم با يکديگر يک يون را مي سازند يون چند اتمي خواهيم داشت. اين يون ها مي توانند کاتيون يا آنيون باشند. آنها با يکديگر پيوند کووالانسي دارند و در واکنشها به صورت واحد مستقل عمل مي کنند
وقتي که دو يا چند اتم با يکديگر يک يون را مي سازند يون چند اتمي خواهيم داشت. اين يون ها مي توانند کاتيون يا آنيون باشند. آنها با يکديگر پيوند کووالانسي دارند و در واکنشها به صورت واحد مستقل عمل مي کنند|
Common Anions | ||
|
Formal Name |
Formula |
Alt. Name |
|
Simple Anions | ||
|
Arsenide |
As3− |
|
|
Azide |
N3− |
|
|
Bromide |
Br− |
|
|
Chloride |
Cl− |
|
|
Fluoride |
F− |
|
|
Hydride |
H− |
|
|
Iodide |
I− |
|
|
Nitride |
N3− |
|
|
Oxide |
O2− |
|
|
Phosphide |
P3− |
|
|
Sulfide |
S2− |
|
|
Peroxide |
O22− | |
|
Oxoanions | ||
|
Arsenate |
AsO43− |
|
|
Arsenite |
AsO33− |
|
|
Borate |
BO33− |
|
|
Bromate |
BrO3− |
|
|
Hypobromite |
BrO− |
|
|
Carbonate |
CO32− |
|
|
Hydrogen carbonate |
HCO3− |
Bicarbonate |
|
Chlorate |
ClO3− |
|
|
Perchlorate |
ClO4− |
|
|
Chlorite |
ClO2− |
|
|
Hypochlorite |
ClO− |
|
|
Chromate |
CrO42− |
|
|
Dichromate |
Cr2O72− |
|
|
Iodate |
IO3− |
|
|
Nitrate |
NO3− |
|
|
Nitrite |
NO2− |
|
|
Phosphate |
PO43− |
|
|
Hydrogen phosphate |
HPO42− |
|
|
Dihydrogen phosphate |
H2PO4− |
|
|
Permanganate |
MnO4− |
|
|
Phosphite |
PO33− |
|
|
Sulfate |
SO42− |
|
|
Thiosulfate |
S2O32− |
|
|
Hydrogen sulfate |
HSO4− |
Bisulfate |
|
Sulfite |
SO32− |
|
|
Hydrogen sulfite |
HSO3− |
Bisulfite |
برای دیدن بقیه بنیانها به ادامه مطلب مراجعه کنید.
ترکيبات يوني در حالتي که يون ها بتوانند آزادانه حرکت کنند رساناي خوبي هستند. اما آنها درحالت جامد فقط داراي حرکت هاي ارتعاشي هستند به همين دليل اين ترکيبات به حالت مذاب و محلول رساناي جريان الکتريسيته مي باشند و يون ها به آساني جريان برق را عبور مي دهند . ترکيبات يوني به دليل داشتن نيروهاي جاذبه قوي از نقطه ذوب و جوش بالايي برخوردارهستند.
بعضي از ترکيبات مثل شکر ملوکولي حل مي شوند و رسانايي الکتريکي ندارند. ان ها در محلول يون ايجاد نمي کنند. فيلم مقايسه حل شدن شکر را با نمک ببينيد.





|
|
| ||||||||||||||||||||
|
بلور نمک طعام |
خنثي بودن نمک طعام |
پيوند يوني، پيوندي است که بر اثر نيروي جاذبه ي ميان يون هايي با بار نا هم ناهمنام تشکيل مي شود.
اين نيروي جاذبه تنها محدود به يک آنيون و يک کاتيون نيست بلکه در تمام جهت ها و ميان همه يون هاي نا همنام مجاور و در فواصل مختلف وجود دارد نيروي جاذبه بين يون هاي با بار ناهمنام خيلي بيشتر از نيروي جاذبه بين يون هاي با بار همنام است. به نحوي که نيروي جاذبه حاصل1/76برابر نيروي جاذبه بين يک جفت يون است.

 |
+ |  |
--> |  |
وقتي اتمي الکترون از دست بدهد به کاتيون تبديل شده و کوچکتر مي شود. اتم کلر الکترون گرفته به آنيون تبديل شده و بزرگتر مي شود. فيلم گرفتن و از دست دادن الکترون را ببينيد.
فيلم هاي ديگري از گرفتن و از دست دادن الکترون توسط کلر و سديم




USGOV.jpg)
|
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
در عناصر واسطه، موقع کندن الکترون ابتدا الکترون از مدار بالا جدا مي شود.
مثلا سدیم با عدد اتمی ۱۱ با از دست دادن ۱ الکترون به آرایش گاز نجیب قبل از خود یعنی نئون می رسد و به سدیم با +۱ تبدیل میشود.

مثلا فلوئور با عدد اتمی ۱۷ با گرفتن ۱ الکترون به آرایش پایه گاز نجیب بعد از خود یعنی آرگون می رسد.

.jpg) به هر يوني که از يک اتم، بر اثر گرفتن يا از دست دادن يک يا چند الکترون تشکيل مي شود. يون تک اتمي مي گويند. يراي مثال عناصر گروه 1 با از دست دادن يک الکترون، کاتيوني با بار +1 و فلزهاي گروه دو با از دست دادن دو الکترون کاتيوني با بار +2 ايجاد مي کنند.براي ناميدن کاتيون تک اتمي پيش از نام عنصر کلمه ي يون را اضافه مي کنيم. مثل يون سديم، براي ناميدن يک آنيون تک اتمي به انتهاي نام نافلز پسوند «يد» اضافه مي کنيم.
به هر يوني که از يک اتم، بر اثر گرفتن يا از دست دادن يک يا چند الکترون تشکيل مي شود. يون تک اتمي مي گويند. يراي مثال عناصر گروه 1 با از دست دادن يک الکترون، کاتيوني با بار +1 و فلزهاي گروه دو با از دست دادن دو الکترون کاتيوني با بار +2 ايجاد مي کنند.براي ناميدن کاتيون تک اتمي پيش از نام عنصر کلمه ي يون را اضافه مي کنيم. مثل يون سديم، براي ناميدن يک آنيون تک اتمي به انتهاي نام نافلز پسوند «يد» اضافه مي کنيم.
يونهاي عناصر واسطه بدون به کار بردن قاعده ي هشتايي پايدار مي شوند. چون مي توانند يونهايي با بار متفاوت ايجاد کنند. بار يون در پرانتز با اعداد يوناني نوشته مي شود
نافلزهاي گروه 16 با به دست آوردن 2 الکترون آنيوني با دو بار منفي و نافلزات گروه 17 با گرفتن يک الکترون آنيوني با بار -1 توليد مي کنند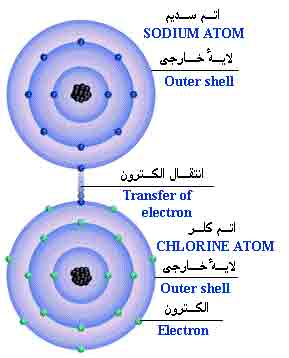






 هشتايي شدن تعداد الکترونهاي موجود در بيروني ترين لايه ي الکتروني (لايه ظرفيت) و دستيابي به آرايش الکتروني گاز نجيب مبنايي براي سنجش پايداري اتم ها و ميزان واکنش پذيري آنها است.
هشتايي شدن تعداد الکترونهاي موجود در بيروني ترين لايه ي الکتروني (لايه ظرفيت) و دستيابي به آرايش الکتروني گاز نجيب مبنايي براي سنجش پايداري اتم ها و ميزان واکنش پذيري آنها است.





نیروی پیش برنده یک واکنش یونی ، جاذبه الکتروستاتیکی متقابل یونهای ناهمنام است. این جاذبه باعث آزاد شدن انرژی شبکه میشود. انرژی شبکه، عامل مهمی در تعیین تعداد بار منفی یا مثبتی است که اتمها به هنگام تشکیل یک بلور یونی میپذیرند.
نامگذاری ترکیبات یونی
نامگذاری ترکیبات یونی بر قواعدی چند استوار است. ابتدا از کاتیون (یون مثبت) ترکیب نام برده میشود و آنیون (یون منفی) پس از آن ذکر میشود.
 |
برخی از فلزات بیش از یک نوع کاتیون بوجود میآورند. در اینگونه موارد ، با نشان دادن تعداد بار کاتیونها در نامشان آنها را متمایز میکنیم. بار این نوع کاتیونها بصورت ارقام لاتین بعد از نام فارسی عنصر قرار داده میشود. +Cu ، یون مس (I) و 2+Cu ، یون مس (II) است. در روشی قدیمیتر برای متمایز کردن دو نوع یون بوجود آمده از یک فلز ، پسوندی به نام فلز افزوده میشود. در این روش ، هرگاه نماد فلزی از لاتین مشتق شده باشد، از نام لاتین فلز استفاده میشود.
پسوند "- و" برای یون دارای بار مثبت کمتر و پسوند "- یک" برای یون با بار مثبت بیشتر مورد استفاده قرار میگیرد. +Cu ، یون کوپرو و 2+Cu یون کوپریک است. +Fe ، یون فرو و 2+Fe یون فریک است.
توجه کنید که در روش بالا تعداد بارها بروشنی بیان نمیشود و نیز این روش برای فلزاتی که بیش از دو نوع کاتیون تولید میکنند، قابل استفاده نیست.
 |
آنیونهای چند اتمی بسیاری شناخته شدهاند. بعنوان مثال 2-O2 یون پراکسید ، Cr2O7-2 یون کرومات ، SO3-2 یون سولفیت و 3-AsO4 یون آرسنات است.
این یون ، یونی است که از چند اتم که با یکدگیر پیوند کووالانسی دارند، بوجود میآید. کایتونهای چند اتمی معدودند و دو نوع نمونه متداول عبارت اند از :
• +NH4 یون آمونیوم و 2+Hg2 یون جیوه (I) یا یون مرکورو.
• یون 2+Hg2 یون جیوه I نامیده شده است. زیرا میتوان آن را متشکل از دو یون +Hg (که با یکدیگر پیوند کووالانسی دارند) در نظر گرفت.
نام ترکیبات یونی ، متشکل از نام کاتیون و پس از آن ، نام آنیون (بصورت لغتی جداگانه) است.
• Fe2O3: آهن (II) اکسید یا فریک اسید.
• PbCO3: سرب (II) کربنات یا پلمبوکربنات.
• NH4)2S): آمونیوم سولفید
• Mg(NO3)2: منیزیم نیترات
• Cu(CN)2: مس (II) سیانید یا کوپریک سیانید
