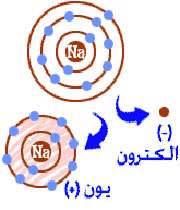
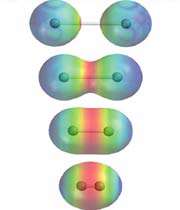
| پیوند یونی جاذبهای است که بین یونهای مثبت و منفی وجود دارد و آنها را در یک ساختار بلورین به هم نگه میدارد. این پیوند ناشی از انتقال الکترون بین اتم هاست. |
پیوند یونی جاذبهای است که بین یونهای مثبت و منفی وجود دارد و آنها را در یک
ساختار بلورین به هم نگه میدارد. این پیوند ناشی از انتقال الکترون بین اتم هاست.

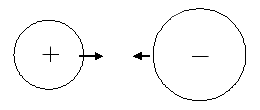
دید کلی
ترکیبات یونی متشکل از تعداد زیادی
آنیون و
کاتیون هستند که با طرح معین هندسی در کنار هم قرار گرفت
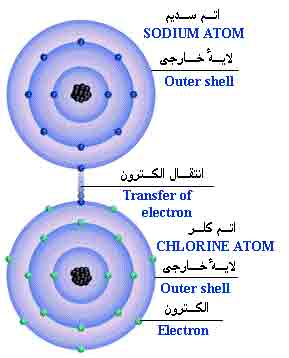
هاند و یک
بلور بوجود میآورند. هر بلور ، به سبب جاذبههای منفی ـ مثبت یونها به هم ، نگهداشته شده است.
فرمول شیمیایی یک ترکیب یونی نشانه سادهترین نسبت یونهای مختلف برای به وجود آوردن بلوری است که از نظر الکتریکی خنثی باشد.
پیوند یونی IonicBond
وقتی اتمها به یون تبدیل میشوند، خواص آنها شدیدا تغییرمیکند. مثلا مجموعهای از مولکولهای
برم قرمز است. اما یونهای
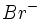
در رنگ بلورماده مرکب هیچ دخالتی ندارند. یک قطعه
سدیم شامل اتمهای سدیم نرم است. خواص فلزی دارد و بر
آب به شدت اثر میکند. اما یونهای
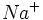
در آب پایدارند.
مجموعه بزرگی از مولکولهای
کلر ، گازی سمّی بهرنگ زرد مایل به سبز است، ولی یونهای کلرید
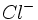
مواد مرکب رنگ ایجاد نمیکنند و سمّی نیستند. به همین لحاظ است که یونهای سدیم و کلر را به صورت نمک طعام میتوان بدون ترس از واکنش شدید روی
گوجه فرنگی ریخت. وقتی اتمها به صورت یون در میآیند، ماهیت آنها آشکارا تغییر میکند.
خواص مواد مرکب یونی
- رسانایی الکتریکی :
رسانایی الکتریکی مواد مرکب یونی مذاب به این علت است که وقتی قطبهایی با بار مخالف در این مواد مذاب قرار گیرد و میدان الکتریکی برقرارشود، یونها آزادانه به حرکت در میآیند. این حرکت یونها بار یا جریان را از یکجا به جای دیگر منتقل میکنند. در جسم جامد که یونها بیحرکتاند و نمیتوانند آزادانه حرکت کنند، جسم خاصیت رسانای الکتریکی ندارد.
- سختی :
سختی مواد مرکب یونی به علت پیوند محکم میان یونهای با بار مخالف است. برای پیوندهای قوی انرژی بسیاری لازم است تا یونها از هم جدا شوند و امکان حرکت آزاد حالت مذاب را پیداکنند. انرژی زیاد به معنی نقطه جوش بالا است که خود از ویژگیهای مواد مرکب یونی است.
- شکنندگی :
مواد مرکب یونی شکنندهاند. زیرا که ساختار جامد آنها آرایه منظمی از یونهاست. مثلا ساختار سدیم کلرید (NaCl) را در نظر بگیرید. هرگاه یک سطح از یونها فقط به فاصله یک یون در هر جهت جابجا شود، یونهایی که بار مشابه دارند درکنار یکدیگر قرار میگیرند و یکدیگر را دفع میکنند و چون جاذبهای در کار نیست بلور میشکند. سدیم کلرید را نمیتوان با چکش کاری ، به ورقههای نازک تبدیل کرد. با چنین عملی بلور نمک خرد و از هم پاشیده میشود.

گروههای حاوی پیوند یونی
یعنی
Li ،
Na ،
K ،
Rb ،
Cs ، هر یک به ترتیب یک الکترون بیشتر از
گازهای نجیب ، (He ، Kr ، Ne ، Ar ، Xe) دارند. اگر هر یک از این فلزات از هر اتم یک
الکترون از دست بدهند، جزء باقیمانده
آرایش الکترونی گاز نجیب متناظر خود را پیدا میکند. مثلا ، Li یک
الکترون والانس در آرایش حالت پایه دارد. از دست دادن یک الکترون موجب میشود که Li
ساختار الکترونی He را پیداکند. یک اتم Li که فقط دو الکترون و سه
پروتون داشته باشد، بار +1 خواهد داشت.
یک اتم باردار مانند

یا یک گروه از اتمهای باردار ، مانند گروه سولفات
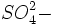
را
یون میگویند.
هریک دو الکترون والانس دارند. پس برای اینکه mg ، ca ، sr ، ba ساختار گاز نجیب را به دست آورند اتمهای هرعنصر باید دو الکترون از دست بدهند. از دست رفتن دو الکترون موجب میشود که دو پروتون در
هسته خنثی نشده بماند. پس هر یون بار +2 خواهد داشت. برای جدا شدن سومین الکترون لازم است جفت الکترونهای تراز اصلی با انرژی پایینتر شکسته شود. این امر انرژی زیادتری میخواهد. جداشدن الکترونها از فلزات و تشکیل یونهای مثبت حاصل از آنها را میتوان به راههای مختلف ترسیم کرد.
پس جدا شدن یک الکترون از یک
اتم معین جداشدن الکترونهای بعدی به ترتیب مشکلتر میشود. زیرا با از دست رفتن هر الکترون بار مؤثر زیادتری میشود و الکترونهای باقیمانده را محکمتر نگاه میدارد. بطور خلاصه یونهای مثبت وقتی تشکیل میشوند که اتمهای فلزی یک الکترون (گروهIA ) دو الکترون (گروهIIA) و یا سه الکترون (گروهIIIA) به اتمهای غیر فلزی میدهند. یونهای حاصل آرایش الکترونی یکسان با یک گاز نجیب دارند.
عناصر گروه VIIA (هالوژنها)
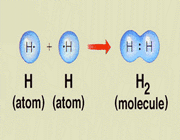
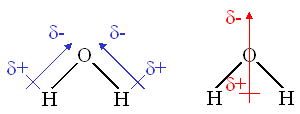
یونهای مثبت در حضور یونهای منفی پایدار میشوند. خنثی شدن بار ، هر دو نوع یون را پایدار میکند. یونهای منفی پایدار ، از اتمهایی که شش یا هفت الکترون والانس دارند، تولید میشوند. اینگونه اتمها آنقدر الکترون بدست میآورند تا ساختار گاز نجیب را پیدا کنند. مثلا اتمهای عناصر گروه
VIIA (هالوژنها) هفت الکترون والانس دارند و هر یک ، یک الکترون میخواهند تا آرایش الکترونی یک گاز نجیب را پیدا کنند.

























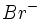 در رنگ بلورماده مرکب هیچ دخالتی ندارند. یک قطعه
در رنگ بلورماده مرکب هیچ دخالتی ندارند. یک قطعه 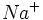 در آب پایدارند.
در آب پایدارند.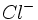 مواد مرکب رنگ ایجاد نمیکنند و سمّی نیستند. به همین لحاظ است که یونهای سدیم و کلر را به صورت نمک طعام میتوان بدون ترس از واکنش شدید روی
مواد مرکب رنگ ایجاد نمیکنند و سمّی نیستند. به همین لحاظ است که یونهای سدیم و کلر را به صورت نمک طعام میتوان بدون ترس از واکنش شدید روی 
 یا یک گروه از اتمهای باردار ، مانند گروه سولفات
یا یک گروه از اتمهای باردار ، مانند گروه سولفات 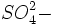 را
را  «معلم شهید محمدجواد حسن زاده » ، شهیدی که مدتی نیست از ما جدا شده و جزو همان شهدایی است که مدتی پیش از این در فضای شهر یا کوچه ما نفس می کشیده و ما غافل از حضور او، غرق دل مشغولی های دنیایی خود بودیم، بدون این که بتوانیم حضور او را حس کنیم . راستی تا به حال هیچ فکر کرده اید چطور می توان حضور یک شهید را حس کرد؟ براستی آیا شهدا را می توان درک کرد؟ مگر این ذهن های زنگ زده دنیایی دیگر جایی برای شهدا در خود باقی گذاشته اند؟ آن قدر غرق شده ایم که از محیط اطرافمان بیگانه ایم .مدیون شهدا و خون کسانی نمانیم که برای راحتی و آسایش ما جان بر کف رخت مردانه ی شجاعت و شهادت پوشیدیند و به اعلا علیین پر کشیدند!!!
«معلم شهید محمدجواد حسن زاده » ، شهیدی که مدتی نیست از ما جدا شده و جزو همان شهدایی است که مدتی پیش از این در فضای شهر یا کوچه ما نفس می کشیده و ما غافل از حضور او، غرق دل مشغولی های دنیایی خود بودیم، بدون این که بتوانیم حضور او را حس کنیم . راستی تا به حال هیچ فکر کرده اید چطور می توان حضور یک شهید را حس کرد؟ براستی آیا شهدا را می توان درک کرد؟ مگر این ذهن های زنگ زده دنیایی دیگر جایی برای شهدا در خود باقی گذاشته اند؟ آن قدر غرق شده ایم که از محیط اطرافمان بیگانه ایم .مدیون شهدا و خون کسانی نمانیم که برای راحتی و آسایش ما جان بر کف رخت مردانه ی شجاعت و شهادت پوشیدیند و به اعلا علیین پر کشیدند!!!