مشخصات و ساختار مواد
مشخصات و ساختار مواد
در این مطلب، برخی مشخصه های اصلی فیزیکی ماده که چگونگی واکنش ماده با تشعشع را تعیین می کند، مورد بررسی قرار می دهیم. اندرکنش های تابشی (هم تابش و هم جذب) برای اتم های منفرد اتفاق می افتد. بنابراین با یک مرور مختصر ساختار اتمی و با تأکید بر این که مشخصه های اتمی، اندرکنش های ماده را تحت تأثیر قرار می دهد، مطلب را شروع کرده و سپس خواص عمومی اتم ها را درون یک ماده مورد بحث قرار می دهیم.
اتم ها از دو قسمت عمده تشکیل شده اند: هسته و پوسته های الکترونی.
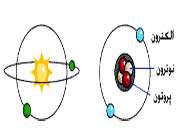
هر ناحیه در اندرکنش های تابشی نقش مهمی ایفا می کند. هسته، منبع انرژی برای تشعشع مورد استفاده در فرایندهای پزشکی هسته ای است. اگرچه هسته منبع انرژی اشعه ایکس نیست اما در تولید فوتون های اشعه ی ایکس نقش دارد. در بسیاری موارد، پرتو تابشی توسط اندرکنش با الکترون های مستقر در پوسته های اطراف هسته جذب می شود. نقل و انتقال در این الکترون های پوسته نیز یک نوع تابش اشعه ی ایکس تولید می کند.
ساختار هسته ای
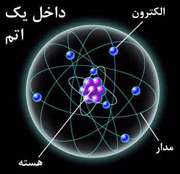
مدلی رایج و قراردادی از یک اتم، از هسته ای که شامل نوترون ها و پروتون هاست و توسط الکترون های مستقر در مدارها یا پوسته های خاصی احاطه شده، تشکیل شده است(در شکل 1 این مدل را مشاهده می کنید). هسته ها به صورت یک توپ یا مجموعه ذراتی در مرکز اتم نشان داده شده اند. هسته در مقایسه با ابعاد کلی یک اتم، کاملاً کوچک است؛ با وجود این، بیش تر جرم اتم درون هسته ی آن جای گرفته است. اجزای اتم در شکل 1 با مقیاس دقیق رسم نشده اند؛ در واقع الکترون ها در لایه های K، L و M بسیار کوچک تر از پروتون ها و نوترون هایی هستند که هسته را می سازند و الکترون ها نسبت به آن چه در شکل نشان داده شده است، در فاصله ی بیش تری از هسته قرار دارند.
ترکیب و نسبت اجزای سازنده ی اتم
تمامی هسته ها از دو ذره ی اساسی تشکیل شده اند: نوترون ها و پروتون ها. نوترون ها و پروتون ها تقریباً اندازه ی مشابهی دارند اما بار الکتریکی آن ها متفاوت است. نوترون ها هیچ باری ندارند و فقط در جرم هسته سهم دارند. هر پروتون، یک بار مثبت دارد که مساوی با قدرت بار منفی حمل شده توسط یک الکترون است.
|
|
|
شکل 1: ساختار یک اتم |
اکثر ویژگی های فیزیکی و شیمیایی یک ماده به ترکیب پروتون- نوترون هسته مربوط است. تعداد پروتون ها در یک هسته، عدد اتمی (Z) نام دارد و خصوصیات شیمیایی اتم را کنترل می کند. هر عدد اتمی با عنصر شیمیایی متفاوتی متناظر است؛ تا کنون تقریباً 106 عنصر شیمیایی شناخته شده که با هسته هایی که شامل 1 تا 106 پروتون هستند، متناظرند.
به دلیل اندازه ی بسیار کوچک هسته، بیان جرم هسته ها و ذرات اتمی با واحد اندازه گیری رایج کیلوگرم، مناسب نیست. یک واحد مناسب تر، واحد جرم اتمی (amu) است؛ این واحد بر اساس مرجع بودن یک اتم کربن با عدد جرمی 12 که با جرم 12000 amu مشخص می شود، پایه گذاری شده است. رابطه ی بین واحد جرم اتمی و کیلوگرم به صورت زیر است:
1 amu = 1.66 x 10-27 kg
تفاوت جرم یک نوترون و پروتون بسار کوچک است: تقریباً 0.1 % . تفاوت بزرگ تر در جرم این دو ذره و جرم یک الکترون است. بیش تر از 1800 الکترون لازم است تا جرمی مساوی با جرم یک پروتون یا نوترون داشته باشد.
تعداد کل ذرات (نوترون ها و پروتون ها) در یک هسته، عدد جرمی (A) نام دارد. از آن جایی که پروتون ها و نوترون ها تقریباً جرم یکسانی دارند، جرم یا وزن کلی هسته (در حدود معینی) متناسب با عدد جرمی است. با این وجود و در حالت کلی، جرم هسته ای با عدد جرمی متناسب نیست زیرا نوترون ها و پروتون ها جرم واقعاً یکسانی ندارند و مقداری از جرم هنگام تشکیل هسته به انرژی تبدیل می شود. رابطه ی بین جرم و انرژی با جزئیات بیش تر در ادامه توضیح داده خواهد شد.
روش استانداردی برای نشانه گذاری و تعیین ترکیبات هسته ای مختلف وجود دارد:
عدد جرمی یا با یک بالانویس قبل از نماد شیمیایی بیان می شود، مانند 14 C یا 131 I و یا توسط عددی که به دنبال نماد شیمیایی می آید، تعیین می شود، مانند C-14 یا I-131 و ... . عدد اتمی به صورت یک زیرنویس پیش از نماد شیمیایی اضافه می شود؛ اما از آن جایی که تنها یک عدد اتمی به هر نماد یا عنصر شیمیایی وابسته است، افزودن عدد اتمی به نماد شیمیایی تا حدودی اضافی است.
به استثنای هیدروژن معمولی، تمام هسته ها شامل نوترون و پروتون هستند. عناصر سبک تر (با اعداد اتمی و جرم کم تر) تقریباً شامل تعداد مساوی پروتون و نوترون هستند. به همان ترتیب که اندازه ی هسته افزایش پیدا می کند، نسبت نوترون ها به پروتون ها به یک مقدار بیشینه ای حدود 1.3 نوترون به ازای هر پروتون برای موادی با اعداد اتمی بسیار بالا افزایش پیدا می کند. تعداد نوترون ها در یک هسته ی خاص می تواند با کم کردن عدد اتمی از عدد جرمی به دست
یک عنصر شیمیایی ممکن است هسته هایی با تعداد متفاوت نوترون نیز داشته باشد که این تغییر در ترکیب نوترونی معمولاً هنگامی که هسته، رادیواکتیو است، پیش می آید.
 برای دریافت بارم بندی شیمی مقاطع متوسطه و پیش دانشگاهی بر روی لینک زیر کلیک کنید
برای دریافت بارم بندی شیمی مقاطع متوسطه و پیش دانشگاهی بر روی لینک زیر کلیک کنید

 دالتون در سال ۱۸۰۳ توانست نظریه اتمی خود را به شکل زیر بیان کند :
دالتون در سال ۱۸۰۳ توانست نظریه اتمی خود را به شکل زیر بیان کند :
 ۴- دموکريت: 2500 سال پيش ، همه مواد از ذره هاي کوچک و تجزيه ناپذيري به نام اتم ساخته شده اند. به نظر او تفاوت مواد در شکل، آرايش و موقعيت اتم آن ها است .
۴- دموکريت: 2500 سال پيش ، همه مواد از ذره هاي کوچک و تجزيه ناپذيري به نام اتم ساخته شده اند. به نظر او تفاوت مواد در شکل، آرايش و موقعيت اتم آن ها است .


 رادرفورد وجود نوترون را نيز حدس زده بود. اما در سال 1932، دانشجوي وي چادويک، وجود ذره خنثي را در اتم به اثبات رسانيد
رادرفورد وجود نوترون را نيز حدس زده بود. اما در سال 1932، دانشجوي وي چادويک، وجود ذره خنثي را در اتم به اثبات رسانيد 









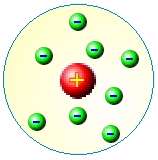
 جورف تامسون، پس از کشف الکترون، مدل اتمي کيک کشمشي يا مدل هندوانه اي خود را ارائه داد.
جورف تامسون، پس از کشف الکترون، مدل اتمي کيک کشمشي يا مدل هندوانه اي خود را ارائه داد.


 جرم يک اتم به تعداد پروتون ها و نوترون هاي آن بستگي دارد. جرم الکترونها قابل چشم پوشي است
جرم يک اتم به تعداد پروتون ها و نوترون هاي آن بستگي دارد. جرم الکترونها قابل چشم پوشي است









 تمام عناصر این گروه در واکنش با آب تولید یک محلول بازی می کنند.( خاکستر چوب مي تواند چربي را در خود حل کند که به آن قليا مي گويند، چون در خاکستر چوب اين فلزات وجود دارد به آنها فلزات قليايي مي گويند).
تمام عناصر این گروه در واکنش با آب تولید یک محلول بازی می کنند.( خاکستر چوب مي تواند چربي را در خود حل کند که به آن قليا مي گويند، چون در خاکستر چوب اين فلزات وجود دارد به آنها فلزات قليايي مي گويند).

 «معلم شهید محمدجواد حسن زاده » ، شهیدی که مدتی نیست از ما جدا شده و جزو همان شهدایی است که مدتی پیش از این در فضای شهر یا کوچه ما نفس می کشیده و ما غافل از حضور او، غرق دل مشغولی های دنیایی خود بودیم، بدون این که بتوانیم حضور او را حس کنیم . راستی تا به حال هیچ فکر کرده اید چطور می توان حضور یک شهید را حس کرد؟ براستی آیا شهدا را می توان درک کرد؟ مگر این ذهن های زنگ زده دنیایی دیگر جایی برای شهدا در خود باقی گذاشته اند؟ آن قدر غرق شده ایم که از محیط اطرافمان بیگانه ایم .مدیون شهدا و خون کسانی نمانیم که برای راحتی و آسایش ما جان بر کف رخت مردانه ی شجاعت و شهادت پوشیدیند و به اعلا علیین پر کشیدند!!!
«معلم شهید محمدجواد حسن زاده » ، شهیدی که مدتی نیست از ما جدا شده و جزو همان شهدایی است که مدتی پیش از این در فضای شهر یا کوچه ما نفس می کشیده و ما غافل از حضور او، غرق دل مشغولی های دنیایی خود بودیم، بدون این که بتوانیم حضور او را حس کنیم . راستی تا به حال هیچ فکر کرده اید چطور می توان حضور یک شهید را حس کرد؟ براستی آیا شهدا را می توان درک کرد؟ مگر این ذهن های زنگ زده دنیایی دیگر جایی برای شهدا در خود باقی گذاشته اند؟ آن قدر غرق شده ایم که از محیط اطرافمان بیگانه ایم .مدیون شهدا و خون کسانی نمانیم که برای راحتی و آسایش ما جان بر کف رخت مردانه ی شجاعت و شهادت پوشیدیند و به اعلا علیین پر کشیدند!!!