بافر
انواع بافرها (بافرهای ترکیبی):
بافرهای ترکیبی به دو گروه بافرهای اسیدی و بافرهای بازی طبقه بندی می شوند:
بافر اسیدی: محلولی از اسید ضعیف و نمک آن در مقابل باز قوی
مثال: H2CO3 + Na2CO3 ، CH3COONa + CH3COOH
بافر بازی: محلولی از باز ضعیف و نمک آن در مقابل اسید قوی
مثال: NH4OH + NH4NO3 و NH4OH +NH4Cl
بافر اسیدی که این جا استیک اسید و نمک آن در مقابل باز قوی ای مثل NaOH می باشد. در محلول بافری هم یون های استیک اسید و هم یون های سدیم استات حضور دارند با این تفاوت که استیک اسید به طور ناچیز یونیزه می شود در حالی که سدیم استات به طور کامل یونیزه می گردد.
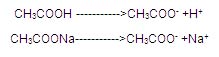
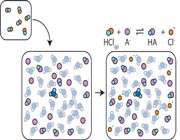
با کلیک بر روی " +Add strong Acid,H " ، افزودن یک اسید قوی را به محلول مورد بررسی قرار می دهیم.
زمانی که یک اسید اضافه می شود، +H از اسید با یون های استات موجود در محلول ترکیب می شود و اسید ضعیف استیک اسید را تشکیل می دهد. بنابراین تغییری در PH صورت نمی گیرد.
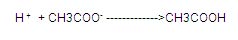
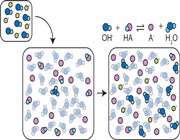
سپس با کلیک بر روی " -Add strong Base ،OH " ، افزودن یک باز قوی را به محلول بررسی می کنیم.
زمانی که یک باز اضافه می شود، -OH از باز با استیک اسید موجود در محلول ترکیب می شود و یون های استات و آب را تشکیل می دهد که به دنبال این امر، باز هم تغییری در PH صورت نمی گیرد.

در کل PH بافرهای اسیدی زیر 7 قرار دارد و در واقع این PH را می توان با استفاده از معادله ی هندرسون بدست آورد:
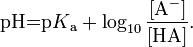
که در این جا منظور از Ka ، قدرت اسیدی و یا ثابت تفکیک اسید می باشد و منظور از [ -A ] غلظت نمک اسید و یا باز مزدوج و [ HA ] غلظت اسید است.
نکته :
معادله ی هندرسون به صورت زیر بدست می آید :
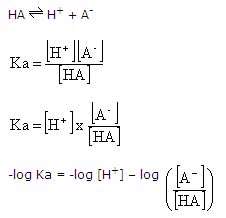

 «معلم شهید محمدجواد حسن زاده » ، شهیدی که مدتی نیست از ما جدا شده و جزو همان شهدایی است که مدتی پیش از این در فضای شهر یا کوچه ما نفس می کشیده و ما غافل از حضور او، غرق دل مشغولی های دنیایی خود بودیم، بدون این که بتوانیم حضور او را حس کنیم . راستی تا به حال هیچ فکر کرده اید چطور می توان حضور یک شهید را حس کرد؟ براستی آیا شهدا را می توان درک کرد؟ مگر این ذهن های زنگ زده دنیایی دیگر جایی برای شهدا در خود باقی گذاشته اند؟ آن قدر غرق شده ایم که از محیط اطرافمان بیگانه ایم .مدیون شهدا و خون کسانی نمانیم که برای راحتی و آسایش ما جان بر کف رخت مردانه ی شجاعت و شهادت پوشیدیند و به اعلا علیین پر کشیدند!!!
«معلم شهید محمدجواد حسن زاده » ، شهیدی که مدتی نیست از ما جدا شده و جزو همان شهدایی است که مدتی پیش از این در فضای شهر یا کوچه ما نفس می کشیده و ما غافل از حضور او، غرق دل مشغولی های دنیایی خود بودیم، بدون این که بتوانیم حضور او را حس کنیم . راستی تا به حال هیچ فکر کرده اید چطور می توان حضور یک شهید را حس کرد؟ براستی آیا شهدا را می توان درک کرد؟ مگر این ذهن های زنگ زده دنیایی دیگر جایی برای شهدا در خود باقی گذاشته اند؟ آن قدر غرق شده ایم که از محیط اطرافمان بیگانه ایم .مدیون شهدا و خون کسانی نمانیم که برای راحتی و آسایش ما جان بر کف رخت مردانه ی شجاعت و شهادت پوشیدیند و به اعلا علیین پر کشیدند!!!